¿Qué es la acidez titulable en alimentos? El análisis de Acide Titulable es el contenido porcentual de ácido presente en el alimento, generalmente, se expresa teniendo como base ácido cítrico o ácido acético, este porcentaje se obtiene por el procedimiento de neutralización del ácido en el alimento utilizando una solución estándar de NaOH y usando el factor correspondiente de la concentración del ácido en la muestra.
¿Qué es hidróxido de sodio (NaOH) o hidróxido sódico?
Este componente utilizado en este tipo de análisis es también conocido como sosa cáustica o soda cáustica, es un hidróxido cáustico usado en la industria (principalmente como una base química).
¿Qué es La fenolftaleína?
Es un compuesto químico orgánico que se obtiene por reacción del fenol (C6H5OH) y el anhídrido ftálico (C8H4O3), en presencia de ácido sulfúrico.
¿Qué es titulación?
La titulación es una técnica de análisis químico consiste en agregar ya sea un ácido o una base de concentración conocida a una sustancia contenida en un recipiente, hasta neutralizar el líquido en estudio, al cual se le agrega un indicador utilizado como señal de neutralización.

¿Qué equipos se utilizan en un Análisis de acidez titulable?
- Balanza analítica
- Bureta Tituladora NaOH
- Fiola de 250 ml
- Plancha agitadora
- Agitador magnético
- Pizetas con agua destilada
- pHmetro
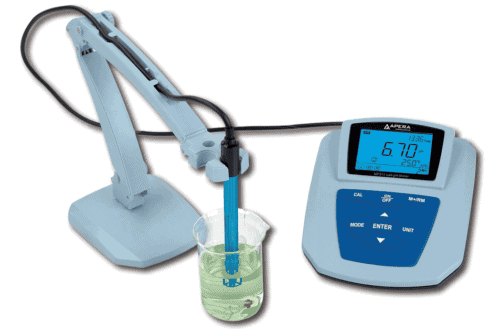
¿Cómo se determina la acidez potenciométrica?
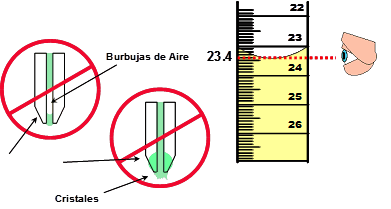
Como calcular el porcentaje de acidez
ECUACION 1:
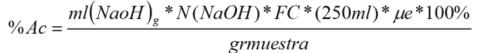
Dónde:
%AC= Porcentaje de ácido o acidez
ml (NaOH)g= Volumen gastado (ml) de NaOH leído en la bureta (ver punto )
N(NaOH) = Normalidad del hidróxido de Sodio real
FC= Factor de Corrección de la solución de NaOH por estandarización según el procedimiento de estandarización de solución NaOH 0.1 N. La ultima formula de esta pagina indica como calcular el factor de corrección.
ue= Mili equivalente de ácido en pulpas:
Manzana y Cereza, ácido málico (ue=0,0067 )
Otras Frutas, ácido cítrico (ue=0,0064 )
Ciruelas y Uva, ácido tartárico (ue=0,0075 )
gr de muestra= gr de pulpa titulado (20 gr)
¿Cómo se determina la acidez titulable?
¿Cómo calcular la acide titulable?
ECUACION 2:
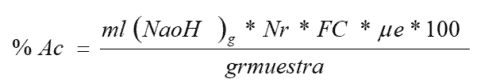
Donde:
%AC= Porcentaje de ácido o acidez
ml (NaOH)g= Volumen gastado (ml) de NaOH leído en la bureta (ver punto )
N(NaOH) = Normalidad del hidróxido de Sodio real
FC= Factor de Corrección de la solución de NaOH por estandarización según el procedimiento de estandarización de solución NaOH 0.1 N
ue= Mili equivalente de ácido en pulpas:
Manzana y Cereza, ácido málico (ue=0,0067 )
Otras Frutas, ácido cítrico (ue=0,0064 )
Ciruelas y Uva, ácido tartárico (ue=0,0075 )
gr. muestra = peso de la muestra real
Nota: Si el ácido a calcular es “ácido cítrico” se puede resumir la ecuación:
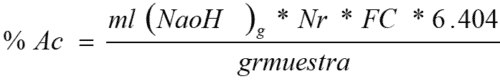
Dónde: 6.04 es el resultado de multiplicar 0.06404*100.
Si la normalidad es igual a 0.1 y vamos a determinar %Ácido Cítrico
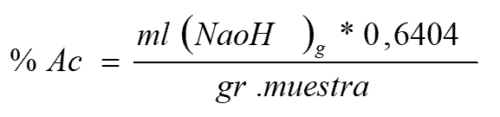
Dónde:
%Ac= Porcentaje de ácido o acidez
mL(NaOH)= Volumen gastado (ml) de NaOH leído en la bureta (paso 24)
Constante= 0.6404 (se obtiene de multiplicar los 0.064040.1N100
gr. muestra = peso de la muestra real
¿Cómo estandarizar el hidróxido de sodio?
¿Formula para determinar la Normalidad del Hidróxido de sodio?
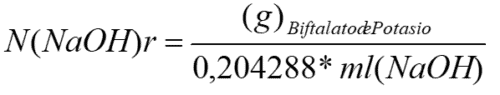
Dónde:
N(NaOH)r = Normalidad real de la solución de NaOH.
(g)Biftalato de Potasio = Gramos de Biftalato de Potasio diluidos.
ml(NaOH)= Mililitros de solución de NaOH leídos en la bureta en el paso.
Determine el factor de corrección con la siguiente ecuación
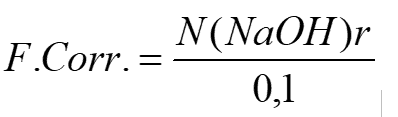
El factor de corrección debe realizarse cada vez que se prepare una bureta de solución.
N(NaOH)r= Normalidad real de la solución de NaOH.
F.Corr = Factor de Corrección.
Rotule la bureta que contiene la solución NaOH ~ 0,1 N indicando el factor de corrección determinado.




